Bei der Verwendung von Gastrennmembranen bestehen prinzipiell zwei Möglichkeiten für die Abtrennung von CO2 (vgl. Abbildung 3). Permeiert CO2 bevorzugt die Membran, fällt ein CO2 reiches Permeat an, das Retentat ist CO2-abgereichert. Im anderen Fall erhält man ein CO2-reiches Retentat und ein CO2-abgereichertes Permeat.
Inhaltsverzeichnis
Für die optimale Verfahrensauswahl bezüglich des Kriteriums Energieverbrauch sind drei Fälle zu berücksichtigen:
- Werden sowohl CO2 als auch die anderen Komponenten des Gemisches als Produkte unter Druck gebraucht, sind für die Auswahl der Variante allein die Eigenschaften (Trennfaktor, Permeabilität; vgl. Kap. 2.2)
- Wird nur CO2 als Produkt benötigt, werden Membranen verwendet, die möglichst kein CO2 permeieren lassen, so dass CO2 im Retentat angereichert wird und nicht mehr komprimiert werden muss.
- In einem Wasserstoffspeichersystem, wie in Abbildung 1 gezeigt, werden bevorzugt für CO2 permeable Membranen eingesetzt, da dadurch das gewünschte Produkt H2 unter Druck anfällt und nicht mehr komprimiert werden muss. Bei mehrstufigen Membrananlagen ist es günstiger eine weniger permeable Gaskomponente im Retentat als die leichter durchdringende im Permeat anzureichern [23C].
Entscheidend für die Auswahl der entsprechenden Variante ist aber die Verfügbarkeit von Membranen mit hoher Selektivität für die jeweilige Trennaufgabe. Ist diese aufgrund der gewünschten Trennleistung nicht gegeben, so muss u.U. die energetisch ungünstigere Variante durchgeführt werden. Im Falle der Aufarbeitung eines H2-haltigen Gemisches für Brennstoffzellen („on board-reforming“, vgl. Kap. 1.3.2) kann die notwendige H2-Reinheit z.Zt. nur mit für H2 hochselektiven Pd-Ag-Membranen erreicht werden.
Für die Auftrennung CO2-haltiger Stoffströme wurde eine Vielzahl von Materialien und Membranarten untersucht, deren chemische Grundlagen nun im folgenden diskutiert werden sollen.
3.1 Siliciumorganische Polymere
In Tabelle 7 sind Beispiele für siliciumorganische Polymere aufgeführt. Polyacetylene und Silicone weisen im Vergleich zu anderen Polymeren um Grössenordnungen höhere Permeabilitäten für Gase auf (vgl. [20], S. 24; [22], S. 85; [28]).
| Membranmaterial | T/°C | Permeabilitätskonstante/barrer | ||||
| O2 | N2 | CO2 | CH4 | H2 | ||
| Poly[1-(trimethylsilyl)-1-propin] (PTMSP) | 25 | 4000 | 2000 | 18000 | 4200 | 6900 |
| Polydimethylsiloxan (PDMS) | 25 | 500 | 250 | 2700 | 800 | 550 |
PTMSP [-CH3C=CSi(CH3)3-]x ist das Polymer mit der z.Zt. höchsten bekannten Permeabilität für Gase. Bei Polyacetylen handelt es sich um ein kristallines Polymer mit einer Glastemperatur von ca. 200 °C (vgl. [29], S. 51). Dieses Polymer weicht von der Tendenz ab, dass glasartige Polymere allgemein eine geringere Gaspermeabilität als gummiartige Polymere besitzen. Als Ursache für diese hohe Permeabilität wird das große freie Volumen [30] seiner Polymerstruktur angenommen.
Das Siliconpolymer PDMS [-Si-(CH3)2-O-]x besitzt eine Glastemperatur von -123 °C und ist damit im Temperaturbereich der Anwendung als Membranmaterial immer gummiartig.
Die Verwendung von PTMSP ist in zahlreichen Laboruntersuchungen publiziert, einer technischen Verwendung des Polymers steht allerdings dessen Alterung unter Verlust der Permeabilität bei Druckbelastung entgegen. PDMS ist ein vielfältig eingesetztes Membranmaterial. Es wird aufgrund seiner hohen Permeabilität und seiner mechanischen, chemischen und thermischen Stabilität u.a. als Schutzschicht und Porenfüller (vgl. Kap. 2.1.1) auf anderen Polymermaterialien eingesetzt.
3.2 Flüssigmembranen
Bei Flüssigmembranen handelt es sich um dünne Filme, die z.B. durch Imprägnieren einer benetzbaren, mikroporösen Membran mit einer Flüssigkeit hergestellt werden (ILM = „immobilized liquid membrane“).
Für die Abtrennung von CO2 kommen Flüssigkeiten in Frage, die aus der konventionellen Absorptionstechnologie bekannt sind (vgl. Kap. 1.3.3). Es werden wässrige Lösungen von Carbonaten, Aminen und Polyethylenglykol [31, 32] oder niedrigschmelzende Salzhydrate (vgl. Literaturzitat Nr. 6-11 in [33]) verwendet. Vorteil der Flüssigmembranen ist, dass gleichzeitig hohe Selektivitäten und Permeabilitäten erreichbar sind. Verglichen mit den Diffusionsköffizienten D in Polymeren von 10 -7 bis 10 -10cm2·s-1 sind diese in Flüssigkeiten mit 10 -5 bis 10 -6 cm2·s-1 um einige Grössenordnungen höher (vgl. Kap. 4.1), was bei ILM auch vergleichsweise hohe Permeabilitäten zur Folge hat. Die erreichbaren Selektivitäten entsprechen denen der Absorptionsprozesse.
Limitierend für den Einsatz von ILM sind die Schwierigkeiten, dünne Trennschichten mechanisch stabil zu erzeugen und die Alterung der Membranen durch Flüssigkeitsverlust. Weiterhin sind die Membranen nur für geringe transmembrane Druckdifferenzen geeignet, da sonst Flüssigkeit aus den Poren gedrückt wird (vgl. Kap. 6.2.1).
3.3 Aminfunktionalisierte Polymere
Die bei den ILM auftretende Schwierigkeit der Membranalterung durch Flüssigkeitsverlust kann man dadurch umgehen, dass man reversibel mit CO2 reagierende Substanzen an das polymere Gerüst anbindet.
Im wesentlichen kommen dafür aminfunktionalisierte Verbindungen in Betracht (zum Mechanismus vgl. Kap. 4.3).
Prinzipiell existieren zwei Konzepte zur Fixierung des Amins, entweder als geladenes Teilchen durch Ionenaustausch an die polymere Matrix (vgl. Kap. 3.3.1) oder durch kovalente Bindung an die Polymerkette (vgl. Kap. 3.3.2).
3.3.1 Kationenaustauscher
Bei der ersten Variante werden als polymere Matrix Kationenaustauscher, als Aminverbindungen monoprotonierte Diamine, Triamine u.s.w. oder als polymere Matrix Anionenaustauscher und Aminosäuresalze (z.B. Glycinat, vgl. [34], S. 340) verwendet. Die Carriersubstanzen werden dann durch elektrostatische Kräfte in der Polymermatrix gehalten. Bei der Verwendung von ionischen Polymeren wird fast immer mit wasserdampffeuchten Gasen gearbeitet, entsprechend sind auch die Polymere in Wasser gequollen.
Variabel bei der Auswahl eines Kationenaustauschers sind das Gerüstpolymer, die Austauschergruppe (überwiegend Sulfonsäuregruppe oder Carbonsäuregruppe), Austauscherkapazität und deren Beladung sowie das Diamin.
Denkbar ist auch die weitere teilweise oder vollständige Quaternisierung der zweiten oder weiterer Amingruppen (z.B. Protonierung und Einführung eines Gegenions) zur Einstellung des pH-Wertes der Polymermatrix (siehe dazu Kap. 3.3.2).
Als Kationenaustauscher wurden mit sulfoniertem Polystyrol gepropftes PTFE, sulfoniertes Polyphenylenoxid (PPO) (vgl. [35], S. 339), Nafion [35, 36, 37] (vgl. Formel 1) und sulfoniertes Styrol-Divinylbenzolpolymer in fluorierter Matrix [38] untersucht.
Way und Kollegen [35, 36] verwendeten als Amin u.a. monoprotoniertes Ethylendiamin (EDAH+). Sie untersuchten die Abtrennung von CO2 aus Mischungen mit CH4 und ternären Gemischen von CO2, CH4 und H2S. Matsuyama et al. haben verschiedene Kationenaustauschermembranen, die durch Plasmapolymerisation von Acrylsäure auf polymeren mikroporösen Substraten erzeugt wurden mit Aminen umgesetzt und deren Permeationseigenschaften für Gase vermessen [39, 40]. Vorteilhaft bei Plasmapolymerisaten ist die Erzeugbarkeit sehr dünner defektfreier Schichten.
3.3.2 Polymere mit kovalent gebundenen Aminen
Bei aminfunktionalisierten Polymeren sind das Gerüstpolymer, der Amingehalt bzw. die Anionenaustauscherkapazität und das polymer angebundene Amin variabel. Variabel ist weiterhin die Quarternisierung der Aminfunktionen (pH-abhängig) und das Gegenion quartärer Ammoniumsalze.
Yoshikawa et al. untersuchten die Wechselwirkungen von CO2 mit polymeren Membranen, die Pyridin als fixierte Carriergruppe enthalten [41]. Als Monomere für die Herstellung von Anionenaustauschern durch Plasmapolymerisation wurden 2-(N,N-dimethyl)aminoethylmethacrylate (DAMA) und Diisopropylamin (DIPA) eingesetzt [42, 43]. Yamaguchi et al. verwendeten Membranen mit Trennschichten aus dem primären Amin Polyallylamin (-(CH2-C(-CH2-NH2H)n-) und Umsetzungsprodukten von Polyallylamin mit 2-Brompropan (vgl. [37], S. 4073).
Membranen aus aminfunktionaliserten Polyimiden wurden aus 3,3′,4,4′-Biphenyltetracarboxyldianhydrid und 2,4,6-Trimethyl-1,4-phenylendiamin durch bromieren der Methylseitengruppen und die Umsetzung mit verschiedenen Aminen hergestellt [44].
Von Yoshikawa [45, 46] et al. und Ballhorn [47] et al. wurden aminfunktionalisierte Polymethacrylathomopolymere (vgl. Formel 2) und Copolymere mit Acrylnitril bezüglich ihrer Gaspermeabilitäten untersucht.

Polymere mit ionischen Gruppen, deren Zahl so groß ist, dass diese wasserlöslich werden, bezeichnet man als Polyelektrolyte [48]. Quinn et al. haben die Verwendung von Membranen aus Polyelektrolyten für die Abtrennung von sauren Gasen aus Gasmischungen untersucht [33, 49]. Sie sind bevorzugt durchlässig für CO2, H2S, COS, SO2 und NOX gegenüber Gasen wie H2, CH4, N2, O2 und CO. Die Membranen bestehen aus einer porösen Unterstruktur, auf der sich eine Polyelektrolytschicht zwischen zwei Schichten aus PDMS oder PTMSP befindet. Es werden quartäre Ammoniumsalze mit Acetat und Fluorid als Gegenion verwendet. Formel 3 zeigt als Beispiele Polyvinylbenzyltrimethylammoniumfluorid (PVBTAF,1) und Poly-N,N-dimethylethyleniminacetat (PDEIAC, 2):

Der Gehalt an funktionellen Gruppen der Polyelektrolyte ist verglichen mit üblichen Ionenaustauschern hoch. Die Ionenaustauscherkapazität (IEC) von PVBTAF beträgt 5,12 Milliäquivalente pro g (meq·g-1), die von PDEIAC 7,62 meq·g-1, in der F– Form sogar 10,97 meq g-1.
PVBTAF weist mit Trennfaktoren α von bis zu 100 (vgl. [33], S. 56) den höchsten bisher bekannten Trennfaktor eines polymeren Materials für CO2/H2 Mischungen auf.
3.4 Hydrogele
Bei Hydrogelen handelt es sich um wassergequollene, vernetzte Polymere, die hydrophil, aber nicht wasserlöslich sind. Am Research Institute of Innovative Technology for the Earth (RITE) werden Hydrogelfilme aus vernetzten Vinylalkohol-Acrylsäuresalzen-Copolymeren untersucht, die in wäßrigen C02-Carrierlösungen gequollen sind [3, 50, 51].
Als Carrier werden dabei Alkalimetallcarbonate oder -bicarbonate eingesetzt, als Additive u.a. aminfunktionalisierte mehrzähnige Komplexliganden für Alkalimetalle (vgl. Formel 4).

Bereits die Zugabe geringer Mengen Additive (Abschätzung: < 0,1 meq Amin·g-1 Polymer trocken) hat erhebliche Effekte auf die Permeabilität für CO2.
Es ist bekannt, dass die Ethylenoxidstruktur eine starke Affinität zu CO2 besitzt (vgl. Literaturzitat Nr. 1-3 in [52]). Deshalb werden vielfach Hydrogele aus Polyethylenoxiden als Membranmaterialien für die CO2-Abtrennung hergestellt. Untersucht sind Polyetherimidcopolymere mit Polyethylenoxid (PEO, wiederholende Einheit Ethylenoxid n = 52) [53], Hydrogele aus plasmavernetzten Polyethylenglykol [3] und UV-vernetzten Polyethylenglykoldimethacrylat und -diacrylaten (n = 23) [52, 54].
3.5 Polyimide
Der Zusammenhang zwischen Polymerstruktur und Gaspermeabilitäten ist gut untersucht [20]. Polyimide besitzen hohe Glastemperaturen (meist > 200 °C).
Die Selektivität dieser Polymere wird weitgehend durch die Diffusion der Gase und nicht durch deren Löslichkeit bestimmt. Im allgemeinen folgt die Permeabilität verschiedener Gase durch Polyimide dem kinetischen Durchmesser (vgl. 20], S. 35, 55, S. 22), d.h. die Permeabilität nimmt in folgender Reihenfolge ab: H2 > CO2 > N2. Somit läßt sich CO2 mit Polymeren dieses Typs zwar aus CO2/N2-Mischungen abtrennen, bei CO2/H2-Mischungen ist aber H2 die wesentlich permeablere Komponente. Kommerzielle Membranen aus Polyimiden haben typische Trennfaktoren CO2/H2 von 0,1 und CO2/N2 von 40 [56].
Konzepte für die Verbesserung der CO2-Permeabilität von Polyimiden sind die Copolymerisation mit PEO (vgl. Kap. Kap. 3.4), die Einführung von Amingruppen (vgl. Kap. 3.3), die Einführung von Gruppen mit möglichst wenigen Rotationsfreiheitsgraden zur Versteifung der Polymerhauptkette (z.B. Bisphenylfluorene, verbunden mit einer Vergrösserung des freien Volumens) oder das Quellen in Aminlösungen [3, 51].
3.6 Sonstige verwendete Membranmaterialien
Polymere, die in konventionellen Modulen verwendet werden, sind: Polyphenylenoxid, Celluloseacetat, Polysulfon, Polybutadien und Polyisopren. Nur die beiden letztgenannten, gummiartigen Polymere zeigen gleichzeitig CO2-Selektivität im Vergleich zu Wasserstoff und Stickstoff.
Härtl, Rompf und Püschel haben die Trennung von CO2/H2-Mischungen bei Drücken bis 400 bar mit Folien aus Polyethylenterephthalat (PET) und Polyamid (PA) untersucht [57, 58]. Wasserstoff ist bei diesen Polymeren die bevorzugt permeierende Komponente.
Sartorelli, Kulcke und Brunner haben bevorzugt CO2-permeable Membranen unter überkritischen Bedingungen eingesetzt. Dabei konnte gezeigt werden, dass Polymermembranen mit Trennschichten aus fluorierten Polymerfilmen bei Drücken von 240 bar und Temperaturen bis 50 °C zur selektiven Abtrennung von CO2 eingesetzt werden können [59].
Anorganische Membranmaterialien werden für die Trennung CO2-haltiger Mischungen dort eingesetzt, wo erhöhte Betriebstemperaturen (> 200 °C) vorliegen. Dabei kommen Silikate, Zeolithe, Kohlenstoff oder Aluminiumoxide zum Einsatz [60, 61]. Die Membranen sind immer bevorzugt für Wasserstoff permeabel.
3.7 Zusammenfassende Beurteilung
Eine Auftragung von Literaturwerten für Permeabilitäten und CO2/N2-Selektivitäten der in Kap. 4.4.1- 4.4.6 besprochenen Polymere ist in Abbildung 7 (Legende vgl. Tabelle 6) gezeigt.
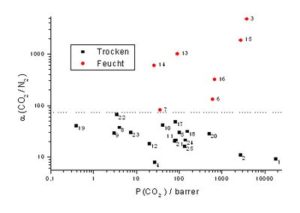
Mit trockenen Membranmaterialien liegen alle Trennfaktoren im Bereich kleiner 70. Werden wassergequollene Membranmaterialien und wasserdampfhaltige Gase eingesetzt, sind um Grössenordnungen höhere Trennfaktoren erreichbar. Herausragend bezüglich Trenneigenschaften sind die Acrylsäurepolymere (Nr. 3, 15, vgl. Abbildung 7).
Dabei handelt es sich um Hydrogele mit hohen Wassergehalten (Nr. 3, 80%). Nr. 15 enthält Kaliumcarbonatlösung als CO2-Carrier und geringe Mengen eines Amins (vgl. Formel 4, Nr. 2).
Nr. 3 besitzt eine sehr hohe IEC (13,1·meq·g-1 trockene Membran) und befindet sich in der EDAH+-Form, welches von verschiedenen Autoren unabhängig als effektivstes CO2-Carrier-Amin in Kationenaustauschermembranen beschrieben ist [37]. Bei Nr. 3 und 15 sind die CO2-Carrier in der Membran frei beweglich, dies führt zu besseren Trenneigenschaften als bei Nr. 6,7,13,14, bei denen die CO2-Carrier (Amine) an das polymere Gerüst fixiert sind. Diese werden jedoch als langzeitstabiler eingestuft, da hier der Carrier nicht aus der Membran „ausbluten“ kann.
Die angegebenen Permeabilitäten und Trennfaktoren nehmen bei Carrier-Membranen mit zunehmendem CO2-Partialdruck im Feed schnell ab (vgl. Kap. 4.3 ), da bei den Carriern Sättigungsphänomene eintreten. Diese Membranen sind deshalb nur im Bereich niedriger CO2-Partialdrücke (vgl. Tabelle 6) effektiv.

In Abbildung 8 sind die Permeabilitäten und CO2/H2-Selektivitäten der beschriebenen Polymere (Legende vgl. Tabelle 6) gezeigt.
Die Trennung von CO2 und H2 mit Membranen ist bisher vergleichsweise wenig untersucht. Die Trennaufgabe ist schwierig, da sowohl H2 als auch CO2 durch Polymere gut permeieren, CO2 aufgrund seiner hohen Löslichkeit in den meisten Polymeren, H2 aufgrund seiner schnellen Diffusion. Trennfaktoren, wie bei CO2/N2, sind daher nicht erreichbar.
Glasartige Polymere (vgl. Abbildung 8, Nr.19, 21, 22, 23, 26) sind für H2 besser permeabel als für CO2. Gummiartige Polymere wie Polybutadien und Polyisopren (Nr. 24,25) trennen C02 aus trockenen CO2/H2-Mischungen mit moderaten Trennfaktoren ab.
PDMS (Nr. 2) ist das Polymer der Wahl zur Abtrennung von CO2 aus trockenen CO2/H2, besitzt aber nur einen idealen Trennfaktor von α ~ 5. Reale Trennfaktoren und Permeabilitäten für Gasgemische sind noch ungünstiger. Angegeben wird ein α (CO2/H2) von 4 bei 1,7 bar Feeddruck (25% CO2) und eine Permeabilität P(CO2) von 762 barrer (vgl.[49], Beispiel 14) oder aber auch „keine Selektivität“ (Prism-Modul) (vgl. [62], S. 3).
Ein literaturbekanntes Beispiel für CO2/H2-Trennfaktoren > 10 sind Polyelektrolyte (vgl. Nr. 14 und 13, Abbildung 8). Die Trennfaktoren sind jedoch sehr stark von einem definierten Wassergehalt der Membranen abhängig und nehmen bei zunehmenden CO2-Partialdruck stark ab.
| Nr | Polymer | T/ °C | p(CO2) Feed / bar | Einzelgas / Gemisch | Feucht / Trocken |
| 1 | PTMSP | 25 | < 1 bar | E | T |
| 2 | PDMS | 25 | 1 | E | T |
| 3 | Plasma Acrylsäure/EDAH+ | 25 | 0,047 | G | F |
| 4 | Polyvinylpyridincopolymer | 30 | – | – | T |
| 5 | DAMA | 25 | 0,047 | – | T |
| 6 | DAMA | 25 | 0,047 | – | F |
| 7 | Aminfunktionalisiertes Polyimid | 25 | 0,36 | G | F |
| 8 | Aminf. Polymethacrylatcopolymer 35:65 | 30 | – | E | T |
| 9 | Aminf. Polymethacrylatcopolymer 20:80 | 30 | – | E | T |
| 10 | Dimethylaminf. Polymethacrylat | 30 | – | E | T |
| 11 | Diethylaminf. Polymethacrylat | 30 | – | E | T |
| 12 | Polymethacrylat | 30 | – | E | T |
| 13 | PVBATF | 23 | 0,11 | G | F |
| 14 | PVBATF | 23 | 0,84 | G | F |
| 15 | Hydrogel Acrylsäurecop. +K2CO3+Additiv | 25 | 0,1 | G | F |
| 16 | Hydrogel Acrylsäurecopolymer + K2CO3 | 25 | 0,1 | G | F |
| 17 | Polyetherimid-PEO-Copolymer | 35 | – | – | T |
| 18 | Polyethylenglykolmethacrylat | 50 | – | – | T |
| 19 | Polyimid | 25 | – | – | T |
| 20 | Bisphenylfluoren-Polyimid | 20 | – | – | T |
| 21 | Polyphenylenoxid | 25 | – | – | T |
| 22 | Celluloseacetat | 25 | -> | – | T |
| 23 | Polysulfon | 25 | – | – | T |
| 24 | Polybutadien | 25 | – | – | T |
| 25 | Polyisopren | 25 | – | – | T |
| 26 | PET | 10 | 50 | G | T |
Für die Realisierung eines Wasserstoffspeichersystems nach Abbildung 1 sind somit noch grundlegende Entwicklungen im Membranbereich notwendig. Reale Trennfaktoren für CO2/H2 im Druckbereich von 10-30 bar (Arbeitsbereich des Speichersystems) mit CO2-selektiven Membranen sind zu messen und Membranen entsprechend zu optimieren.
Schlüssel für die Membranentwicklung ist das Verständnis der Transportmechanismen für CO2 in der Membran und vor allem dessen Zusammenhang mit der Wasserbilanz im System Membran-Gasphase.
Aussichtsreiche Untersuchungsmaterialien könnten gummiartige, aminfunktionalisierte, hygroskopische Polymere sein.
