Inhaltsverzeichnis
CO2 hat als energetisch stabilste Kohlenstoffverbindung eine Schlüsselrolle im natürlichen Kohlenstoffkreislauf. In der Atmosphäre befinden sich ca. 2,7·1012 t CO2, davon sind jährlich 8,1·1011 t im Umlauf. Größere Reservoire für CO2 als die Atmosphäre sind die tiefen Ozeane mit 1,4·1014 t sowie Sedimente mit 2,4·1017 t. Aufgrund anthropogener Einwirkungen erhöht sich die in der Atmosphäre vorhandene Menge jährlich durch Verbrennungsprozesse um 1,85·1010 t, durch Wald- und Bodenzerstörung um weitere 7,4·109 t [1].
Da als Folge dieser raschen Änderung der Atmosphärenzusammensetzung Klimaveränderungen mit erheblichen Auswirkungen erwartet werden, wird nach Wegen gesucht, den CO2-Ausstoß zu reduzieren bzw. CO2-emissionsneutrale Prozesse einzuführen. Um z.B. bei der Nutzung fossiler Brennstoffe zu einem CO2-neutralen Prozess zu kommen, ist als Verfahrensschritt immer eine Abtrennung bzw. Aufkonzentrierung von CO2 notwendig. In weiteren Schritten muss sich die Verwertung des erzeugten CO2 anschließen. Die z.Zt. chemisch verwertbare CO2-Menge von 3,7·107 t CO2 pro Jahr ist aber vergleichsweise gering. In Deutschland werden in der chemischen Industrie nur 0,1% des insgesamt emittierten CO2 benötigt [2].
Somit ist langfristig eine wesentliche Reduzierung der CO2-Emissionen hauptsächlich nur durch die Bildung neuer Kreislaufsysteme, wie die Synthese von gasförmigen oder flüssigen Energieträgern aus CO2, in Kombination mit einer Wasserstofferzeugung über regenerative Energien, machbar [3]. Die chemische Speicherung von Wasserstoff ist dabei, wie auch die konventionelle Erzeugung von Wasserstoff, bei den derzeit geplanten Konzepten immer mit C1-Chemie (Verbindungen mit einem C-Atom) gekoppelt.
Während solche komplexen und vielstufigen Kreislaufprozesse erst in den nächsten Jahrzehnten realisiert werden können, sind einfachere Verfahren, bei denen die Abtrennung von CO2 zu einer direkten Wertschöpfung führt, bereits technisch etabliert. Bei der Aufarbeitung saurer Erdgase zu Pipeline-Qualität (CH4 mit < 2 mol% CO2) sind Membranverfahren zur Abtrennung von CO2 die ökonomischsten Verfahrensvarianten [4]. Die Überprüfung der Implementierbarkeit von Membrantrennverfahren in oben genannte Kreislaufsysteme erscheint daher sinnvoll.
1.2 Zielsetzung
Die für eine solche Trenneinheit erforderlichen Membranen für die CO2-Anreicherung sollen im Rahmen dieser Arbeit hergestellt werden. Weiterhin sind für die Charakterisierung der Membranen Untersuchungsmethoden für die Bestimmung von Transportparametern auszuarbeiten, bzw. bekannte Methoden den Rahmenbedingungen der untersuchten Anwendungsbeispiele anzupassen.
Der konzeptionelle Ansatz dieser Arbeit ist es, aminfunktionalisierte Polymere als Trennschicht für Membranen zu verwenden. Solche Polymere reagieren reversibel mit CO2 und können somit CO2 bevorzugt permeieren lassen. Die unterschiedlichen Effekte von kovalent gebundenen im Vergleich zu ionenausgetauschten Aminogruppen sollen dabei untersucht werden. Im Weiteren soll versucht werden, Membranchemie und Transportprozesse im Rahmen von Untersuchungen des Transportmechanismus miteinander zu korrelieren.
1.3 Stand der Technik – Hintergrund
1.3.1 Wasserstoffspeicherung
Bekannt sind Speicherverfahren wie Druckbehälter für Wasserstoffgas in der Chemieindustrie und Kryotanks für flüssigen Wasserstoff in der Raumfahrt. In der Entwicklungsphase befinden sich neue Speichermethoden wie Metallhydride und Kryoabsorber, siehe dazu auch Tabelle 1 [5]:
| Speichermethode | Ausführung | Anwendung | Betriebstemperatur/ °C |
| Flüssigwasserstoff | Isolierter Tank | mobil, stationär | -252 |
| Kryoabsorber | Aktivkohle u.a. | stationär | -208 |
| Metallhydrid | FeTi u.a. | mobil, stationär | 40 bis 300 |
| Druckbehälter | Drucktank / Untertagespeicher | stationär | frei wählbar |
Bei chemischen Speichern wird Wasserstoff in Form einer wasserstoffreichen Verbindung gelagert.
| Enthaltenes H2-Volumen (Lagertemperatur) Nm3·m-3 | Flüssig von/bis °C | Energiespeicherdichte bei Lagertemperatur kWh·m-3 Speicher | |
| Benzin (Heptan) | 1182 (20 °C) | -90 / 98 | 11000 [5] |
| Methanol | 1100 (25 °C) | -98 / 64 | 4300 [5] |
| Ammoniak (flüssig) | 1672 (-33 °C) | -78 /-33 | 4207 |
| Ameisensäure | 594 (20 °C) | 8 / 101 | 1937 |
| Wasserstoff (100 bar) | 100 (0 °C) | – | 300 |
| Wasserstoff (flüssig) | 793 (< -252 °C) | < -252 | 2380 [5] |
In Tabelle 2 sind erreichbare Energiespeicherdichten in Form der stöchiometrisch enthaltenen Menge an Wasserstoff aufgeführt, zum Vergleich sind die Verbrennungsenthalpien auf das Speichervolumen bezogen angegeben.
Es ist erkennbar, dass die mit chemischen Verbindungen erreichbaren Speicherdichten sowohl bezüglich der enthaltenen Wasserstoffmengen als auch der Verbrennungsenthalpien wesentlich über denen von Druck- oder Tieftemperaturspeichern liegen.
1.3.2 Diskussion der Verfahrensvarianten am Beispiel Fahrzeugantriebe
Wie aus Kap. 1.3.1 ersichtlich ist, beinhalten chemische Wasserstoffspeicher die höchsten Energiedichten. Eine hohe Energiedichte ist bei Fahrzeugen gewünscht, um mit dem vorhandenen Tankvolumen möglichst große Reichweiten zu erzielen. Bei konventionellen Verbrennungsmotoren ist die Verbrennungsenthalpie pro Volumen wesentlich, bei Brennstoffzellenfahrzeugen, die Wasserstoff durch Reformingprozesse erzeugen, die stöchiometrisch enthaltene Menge Wasserstoff, abzüglich Reformingverlusten. Die Wasserstofferzeugung aus Methanol „on-board“ von Fahrzeugen wird momentan zur Serienreife gebracht [6]. Methanol wird als Speicherform für automobile Anwendungen favorisiert, da nur geringfügige Modifikationen der bestehenden Infrastruktur zur Verteilung von Kraftstoffen notwendig sind, eine relativ hohe Energiespeicherdichte vorliegt und der Flüssigtemperaturbereich von Methanol dem konventioneller Kraftstoffe nahe kommt.
Nachteilig ist, dass beim Reformingprozess zur Erzeugung von Wasserstoff aus Methanol CO entsteht (vgl. Gl. 1), welches bis auf Spuren (< 200 ppm) aufwendig abgetrennt werden muss, da übliche Anodenkatalysatoren von Brennstoffzellen durch CO vergiftet werden.
![]()
Auch die Einbeziehung von Methanol in ein CO2-Kreislaufsystem (vgl.Kap. 1.2
, [3]) hat den Nachteil zur Folge, dass aus dem stöchiometrischen Verhältnis der Edukte (bei CO2: n(C)/n(O) = 2) und des Produktes Methanol (CH3OH: n(C)/n(O) = 1) zwangsläufig folgt, dass (vereinfacht) pro Methanol ein Äquivalent H2 zu Wasser umgesetzt wird (vgl. Gl. 2).
![]()
Direkt-Brennstoffzellen z.B. für Methanol oder Formiat sind vielfach untersucht, aber technisch oder in Serienprodukten noch nicht realisiert [7, 8], da bisher geeignete billige, serientaugliche und CO-tolerante Elektrodenmaterialien fehlen.
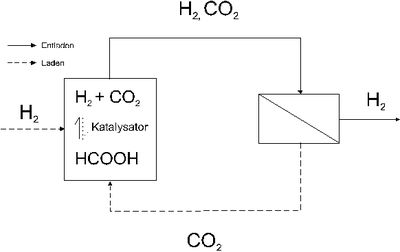
Trotz der geringeren Energiespeicherdichte (vgl. Tabelle 2) von Ameisensäure ist diese für ein CO2-Kreislaufsystem (vgl. Abbildung 1) und eine Verwertung in mobilen Brennstoffzellensystemen interessant, da sie das einzige stöchiometrische Umsetzungprodukt eines Moleküls Wasserstoff mit einem Molekül CO2 (vgl. Gl. 3) ist und bei der Zersetzung kein CO entsteht.
![]()
Bei der Zersetzung von Ameisensäure fällt ein äquimolares Gemisch von CO2 und H2 an. Um Wasserstoff unter Systemdruck zu erhalten und bei Folgeprozessen nicht wieder Kompressionsenergie aufwenden zu müssen, ist eine Prozessführung sinnvoll, bei der selektiv CO2 aus der Mischung abgetrennt wird.
Des weiteren hängt die elektromotorische Kraft einer Brennstoffzelleneinheit (Potential) u.a. vom H2-Partialdruck ab (Nernstsche Gleichung), d.h. mit Erhöhung des Partialdrucks steigt die erreichbare Zellspannung an. Für eine Verwendung von H2 in Brennstoffzellen ist eine Anreicherung auf > 95% notwendig, da Inertgase aus dem Zellsystem ausgeschleust werden müssen und dies immer zu Brennstoffverlusten führt. Beim Prozess Ameisensäure-Trenneinheit-Brennstoffzelle (vgl. Abbildung 1) ist es deshalb notwendig, CO2 von H2 zu trennen.
1.3.3 Verfahrensalternativen zur Abtrennung von CO2
Verfahren für die Abtrennung von CO2 sind Absorption, Kondensation, Druckwechseladsorption (PSA) und Membranverfahren. Absorptionsverfahren zur Abtrennung von CO2 verwenden als Sorbentien verschiedene Amine (Absorptionsprinzip: chemisch) oder Lösemittel, wie z.B. Polyethylenglykoldimethylether oder Propylencarbonat (Absorptionsprinzip: physikalisch) [9].
Die Abtrennung von CO2 mittels Kondensation ist als Verfahrensvariante interessant, wenn die Mischung überwiegend aus CO2 besteht. Voraussetzung dafür ist, dass keine weiteren Substanzen die flüssige Phase verunreinigen.
CO2/H2-Mischungen, wie sie bei der Wasserstofferzeugung durch katalytische Dampfspaltung von Kohlenwasserstoffen und anschließender Konvertierung mit Wasser anfallen, werden üblicherweise durch PSA getrennt [10]. Die neben Wasserstoff in wasserstoffhaltigen Feedgasen vorliegenden Komponenten werden bei höheren Drücken (6-35 bar) mehr oder weniger stark an Adsorbentien (Molekularsiebe) gebunden. Die maximale Beladung wird je nach Adsorbens bei 6-35 bar erreicht (Sättigungsbereich, Langmuir-Charakteristik), eine weitere Druckerhöhung ist somit für den Prozess nicht vorteilhaft. Mit der PSA lassen sich Produktreinheiten von über 99,99% erreichen. Das Produkt Wasserstoff fällt nahezu mit dem Eingangsdruck an. Für den Prozessschritt Druckaufbau ist aber jeweils die Kompressionsenergie einzubringen. Technische Anlagen sind in der Größenordnung von 50-100000 m3·h-1 Wasserstoff realisiert (Mindestgröße von 1-2 m3·h-1[11]).
Die Gastrennung mit Membranen nutzt die unterschiedlichen Permeabilitäten von Gasen durch Membranmaterialien. Triebkraft für den Transport einer Komponente durch die Membran ist deren Partialdruckdifferenz über die Membran. Membranverfahren für die Abtrennung von CO2 werden bei der Aufbereitung von Erdgas zu Pipeline-Qualität, bei der Erdölgewinnung (Enhanced oil recovery), zur Kapazitätserweiterung von Absorptionsanlagen und bei der Aufarbeitung von Deponie- und Biogas eingesetzt [12]. Membranverfahren sind für den Prozessschritt der Abtrennung von CO2 aufgrund ihrer Kompaktheit, ihres modularen, einfachen Aufbaus und geringen Gewichts bei mobilen Anwendungen anderen Verfahrensalternativen überlegen. Des weiteren haben Membrananlagen nahezu keine Mindestgröße, sind ohne Probleme mit variablen Durchsätzen fahrbar, kommen ohne bewegte Teile aus und arbeiten unabhängig von der Einbaulage. Im Weiteren sollen daher Membranen und Membranverfahren für die selektive Abtrennung von CO2 diskutiert werden.
