Inhaltsverzeichnis
- 1 7.1 Messungen mit Einzelgasen
- 2 7.1.1 Nafion 117-EDAH+-Membran
- 3 7.1.2 Anionenaustauscherpolymere
- 4 7.1.2.1 Membran Typ C3
- 5 7.1.2.2 Membran Typ C1
- 6 7.2 Messungen mit Gasgemischen
- 7 7.2.1 Anionenaustauscher Typ H3
- 8 7.2.2 Anionenaustauscher Typ C4
- 9 7.2.2.1 Bestimmung von Aktivierungsenergien
- 10 7.2.3 Laminate aus PDMS und Anionenaustauschern
- 11 7.3 Widerstandsmessungen
Im folgenden Kapitel werden Ergebnisse ausgesuchter Transportmessungen von in den vorherigen Kapiteln diskutierten Polymersystemen vorgestellt und mit den aufgrund von Transportmodellen zu erwartenden Tendenzen verglichen. Wesentliche Einflußgrößen und Wege zur Membranoptimierung und die Grenzen einer Membrantrenntechnik für C02/H2 werden aufgezeigt. Mit den in Kapitel 5 beschriebenen Synthesemethoden steht für die Lösung der im Rahmen dieser Arbeit zu untersuchenden Trennaufgabe eine große Zahl verschiedener Polymermaterialien zur Auswahl. Die Polymere lassen sich in zwei Klassen einteilen: Erstens in kationenaustauschende Polymere, an die monoprotonierte Amine durch Ionenaustausch gebunden sind. Zweitens in anionenaustauschende Polymere, die kovalent gebundene Aminfunktionen enthalten.
Aus den in Frage kommenden Polymeren müssen sich leicht und reproduzierbar Membranen herstellen lassen (Filmbildung, mechanische Eigenschaften), die Membranen müssen permeabel, selektiv und stabil (konstante Permeabilitäten) sein.
In Rahmen von Untersuchungen der vorliegenden Arbeit hat sich herausgestellt, dass die kationenaustauschenden Polymere nur für den Einsatz bei niedrigen Drücken geeignet sind. Bei höheren Drücken trocknen sie aus und es kommt zu Aminverlust, nach einigen Tagen sind die Membranen unbrauchbar. Im weiteren wird daher nur aminmodifiziertes Nafion als Referenzmaterial diskutiert.
An anionenaustauschenden Polymeren werden auf Polyvinylalkohol und auf Polyepichlorhydrin basierende Typen untersucht. Polyepichlorhydrinderivate, besonders Umsetzungsprodukte mit Epichlorhydrin, sind gummiartige Polymere, im Gegensatz zu Polyvinylalkoholderivaten, die dem glasartig sind. Bezüglich der CO2/H2-Trenneigenschaften sind gummiartige Polymere besonders vorteilhaft (vgl. Abbildung 47). Daher werden die Eigenschaften von Polyepichlorhydrinderivaten im weiteren ausführlich diskutiert.
7.1 Messungen mit Einzelgasen
Die Permeationsdaten für Einzelgase werden mit der Druckanstiegsmethode (vgl. Kap. 6.1.1–Kap. 6.1.2) ermittelt.
7.1.1 Nafion 117-EDAH+-Membran
Das System Nafion-EDAH+ ist bezüglich seiner Gastrenneigenschaften vielfach bei geringen CO2-Partialdrücken und transmembranen Partialdruckdifferenzen (Umgebungsdruck, δp max. 1 bar) untersucht worden [108, 34, 35, 36] und wird deshalb im Rahmen dieser Arbeit u.a. als Referenzmaterial – mit den unten genannten Einschränkungen – zur überprüfung von Messmethoden verwendet. Des weiteren soll das Verhalten solcher Membranen bei höheren CO2-Partialdrücken untersucht werden.

In Abbildung 30 ist der Verlauf eines Druckanstiegsexperiments (vgl. Kap. 10.6.1, Nr. 1) gezeigt. Dabei ist jeder 200ste Messpunkt angegeben.
Bei einem konstanten Feeddruck von 3 bar CO2 (100% relative Feuchte) steigt der Permeatdruck nach Messbeginn kontinuierlich an. Die numerische Auswertemethode, die in dieser Arbeit verwendet wird (vgl. Kap. 6.1.1), ergibt im stationären Bereich (vgl. Abbildung 1, ca. 500-8000 s) im Rahmen der Messgenauigkeit vergleichbare mittlere Permeationsraten wie die literaturbekannte analytische Lösung.
Sie gibt aber die Vorgänge im „time lag“ (0-500 s) und Sättigungsbereich (> 8000 s, Erklärung s.u.) besser wieder. Der Anfangsbereich des Druckanstiegs (vgl. Abbildung 2) wird zur Bestimmung des Diffusionskoeffizienten herangezogen (vgl. Kap. 6.1.2).
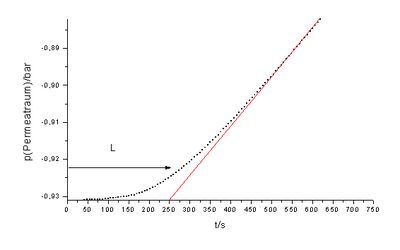
Die Ermittlung der Permeationsraten erfolgt durch Mittelwertbildung über die Messwerte im stationären Bereich der Messung. Dieser Bereich wird für jede Messung anhand der Auftragung des Permeatflusses gegen die Zeit grafisch ermittelt. Im allgemeinen werden Permeationsmessungen nach ca. 5000 s abgebrochen. Die Ergebnisse einer Messserie sind in Anhang (Kap. 10.6.1) aufgelistet.
Die Messungen zeigen, dass mit Nafion-EDAH+-Membranen ideale Trennfaktoren α (CO2/H2) von 5 (3 bar Feeddruck, 30 °C, feuchtegesättigte Gase) erreichbar sind. Bei Temperaturerhöhung auf 60 °C sinkt der Trennfaktor α(CO2/H2) auf 3,9. Die Permeabilität für CO2 steigt bei Temperaturerhöhung von 30 auf 60 °C um das 1,6fache.
Die ideale Selektivität α(CO2/N2) liegt bei 35 (30 °C, 3 bar Feeddruck, feuchtegesättigte Gase). Wird die Membran getrocknet, sinkt die Permeabilität der Membran für wasserdampfgesättigtes CO2 irreversibel auf 20% der ursprünglichen Permeabilität. Der Trennfaktor α(CO2/H2) sinkt auf 0,6.
Es liegt nahe, dass in der Membran als Salz gebundenes Amin, das für den CO2-Transport nötig ist, flüchtig ist und die Membran dann in der H+-Form vorliegt.
Die völlig trockene Membran zeigt zunächst für Kohlendioxid nur noch 0,4% der Permeabilität wie im feuchten Zustand, im Laufe weiterer Messungen steigt die Permeationsrate aber um das Dreifache. Spuren von Wasser führen zu erheblichen Veränderungen im Permeationsverhalten. Messungen für CO2 „trocken“ bedürfen deshalb besonderer experimenteller Maßnahmen, wie die vollständige Trocknung der Messgase und der Durchführung der Messung im Trockenschrank statt im Wasserbad. In Tabelle 13 sind Permeabilitäten und Diffusionskoeffizienten aus Einzelgasmessungen und daraus berechnete Gaslöslichkeiten im Polymer verglichen.
| P (barrer) | P Mittelwert aus Messung Nr. (Vgl. Kap. ) | D·1011/m2·s-1 | S·102/Ncm3·cm-3 (Polymer) ·cmHg-1 | |
| CO2 | 652 | 2-4.4 | 2,7 | 24,1 |
| H2 | 125 | 12.1 | 81 | 0,15 |
Die Diffusionskoeffizienten für H2 sind 30 mal höher als die für CO2, die Löslichkeit von CO2 in der Membranmatrix ist jedoch 160 mal größer als die von Wasserstoff, d.h. die Selektivität der Membran für CO2 ist durch die gute Löslichkeit von CO2 bedingt.
Die bestimmten Diffusionskoeffizienten stimmen von der Größenordnung her mit Literaturwerten überein, die durch Leitfähigkeitsmessungen ermittelt wurden (5,7·10 -11m2·s-1 (25 °C) für Nafion117-EDA+, vgl. [77], S. 4784).
Die publizierten Trennfaktoren α(CO2/H2) für Nafion117-EDA+ liegen zwischen 8-14 bei 0,1 bar CO2 Partialdruck im Feed und sinken für steigende Drücke auf ca. 6 (0,75 bar CO2) [108].
Nach dem in Kap. 4.3.3 vorgestellten Modell (vgl. Abbildung 11) ist für Nafion117-EDAH+ ab einer Partialdruckdifferenz von 1 bar CO2 der Anteil des reaktiven Transportes vernachlässigbar und die Trennfaktoren bleiben bei zunehmender Partialdruckdifferenz nahezu konstant. Somit stimmt auch der gefundene Trennfaktor mit den Literaturwerten überein.
Bekannt ist auch, dass die Permeationsraten für CO2 in Membranen, wenn parallel zum Lösungs-Diffusions-Transport reaktiver Transport vorliegt, vom Verhältnis des Permeat zum Feeddruck abhängig sind (vgl. [77], S. 4787, Fig. 9). Liegt kein reaktiver Transport vor, verläuft die Auftragung des Permeatflusses/ Nm3·m2·h-1 linear bzgl. des Verhältnisses von Permeat- zu Feedpartialdruck, bei reaktivem Transport liegen die Permeatflüsse bei niedrigen Permeat- zu Feedpartialdruckverhältnis höher. D.h. bleibt der auf die Partialdruckdifferenz normierte Permeatfluß im Laufe des Druckanstiegsexperiments (Verhältnis Permeat/Feedpartialdruck nimmt ab) nicht konstant, sondern nimmt ab (vgl. Abbildung 30, Sättigungsbereich) ist dies ein Nachweis für das Vorliegen eines reaktiven Transportmechanismus.
Ein Vergleich der Messergebnisse dieser Arbeit mit publizierten Permeationsraten bedarf einer sorgfältigen Berücksichtigung der Messbedingungen. Die publizierten CO2 Permeationsraten für Nafion117-EDA+ liegen je nach Differenz der CO2-Partialdrücke Feed/Permeat zwischen 1000 (Δp = 0,03 bar) und 300 (Δp = 0,8 bar) barrer (25 °C, Spülgasbetrieb, Feeddruck = Umgebungsdruck, 25 °C) (vgl. [112], S. 217). Der Kurvenverlauf läßt bei weiterer Partialdruckdifferenzzunahme nur noch auf ein geringes Abnehmen der Permeabilität/barrer schließen.
Experimentell ist der CO2-Permeatfluß durch Nafion117-EDAH+-Membranen bei 25 °C zu (4,254 + 2,5 ·Feeddruck)·10-9 / mol·cm-2·s-1 als Grenzwert für ein Verhältnisses von Permeat- zu Feedpartialdruck gegen Null und CO2-Partialdrücke im Feed > 0,1 bar bis 0,84 bar bestimmt worden (vgl. [77], S. 4786, Fig. 4).
Hochgerechnet auf einen Feeddruck von 3 bar ergäbe sich daraus ein maximaler Wert für die CO2-Permeabilität von 922 barrer.
Die gefundenen Messwerte liegen in diesem in der Literatur angegebenen Bereich zwischen 300 und 900 barrer. Diese Streubreite für Permeationswerte ist aufgrund der extremen Abhängigkeit der Messergebnisse von Messbedingungen und Polymerhistorie in der üblichen Größenordnung.
Die Polymerhistorie spielt beim Permeationsverhalten von Nafion eine wesentliche Rolle. Konstante Polymereigenschaften nach änderung von Umgebungsbedingungen stellen sich erst nach Stunden oder Tagen ein.
Bei der Durchführung mehrerer Messungen bei gleicher Temperatur und gleichem Druck (vgl. Kap. 10.6.1, Messung 1-4.1) werden bei der ersten Permeationsmessung nur 50% der Permeationsrate der späteren Messungen erreicht. Nach Messungen bei höheren Temperaturen (80 °C, Messung 10.4) steigen P (um 50%) und D bei niedrigeren Temperaturen an (20 °C, Messung 9, 11.1). Nach dem Quellen in 220 °C (bzw. 100 °C) heißem Glyzerin finden Pelligirino et al. (vgl. [108], S. 217) 40 fach (bzw. 8 fach) höhere Permeationsraten für Nafion117. Dieses Verhalten wird durch eine Aufweitung der inneren Struktur erklärt, so dass in den Kanälen wandernde Teilchen geringe Reibungsverluste erleiden (vgl. [77], S. 4785). Bei der Bestimmung des Qüllverhaltens (wc) von Nafion bei 60 °C daürt es Tage, bis ein in destilliertem Wasser befindliches Membranstück ein konstantes Gewicht aufweist.
dass die Zeitskala für die Einstellung konstanter Polymereigenschaften bei Nafion/CO2 wesentlich länger ist als ein einzelnes Permeationsexperiment ist vor allem für die Bestimmung von D und S mit „time lag“-Experimenten ein Problem. Voraussetzung für die Durchführung des Experiments ist, dass die Probe kein CO2 enthält, da sonst zu kurze „time lag“-Zeiten gefunden werden. Somit ergibt sich D für ein Polymer im Ausgangszustand. Konstante Permeationswerte für C02, die deutlich von den Anfangswerten abweichen, erhält man aber erst für ein Polymersystem, bei dem die CO2-Quellung den Sättigungszustand erreicht hat. Entsprechend groß sind die Unsicherheiten in diesem Fall für die Bestimmung von S (vgl. Tabelle 13).
Aufgrund dieses Verhaltens von Nafion sind die in dieser Arbeit durchgeführten temperaturabhängigen Messserien für eine kinetische Auswertung (Arrhenius-Ansatz) nicht aussagefähig und damit nicht geeignet.
Wie die Messungen zeigen, ist Nafion117-EDAH+ für die Trennung von C02/H2 bei höheren Drücken nicht brauchbar. Aufgrund der relativ geringen IEC kommt es schon bei geringen CO2-Partialdrücken zur kinetischen Hemmung des reaktiven CO2– Transports. Da bei höheren Drücken der Stoffmengenanteil von Wasser in der wassserdampfgesättigten Gasphase abnimmt, ist auch eine Abnahme des Wassergehaltes in der Membran mit zunehmendem Druck zu erwarten (vgl. Kap. 8). Eine Trocknung der Membran führt aber zu irreversiblen Selektivitätsverlust.
Nafion quillt, da es unvernetzt ist, relativ stark und zeigt starke Abhängigkeiten und Hysteresen im Permeationsverhalten, was seine Verwendung in Anwendungen mit starken Schwankungen von Zusammensetzungen und Auslastung (z.B. mobile Anwendungen) ausschließt.
7.1.2 Anionenaustauscherpolymere
7.1.2.1 Membran Typ C3
Bei der Trennschicht der verwendeten Membran handelt es sich um ein Umsetzungsprodukt von Polyepichlorhydrincöthylenoxid mit Polyethylenimin. Dabei beträgt das molare Cl-N Verhältnis 21:1, die IEC 0,34 meq·g-1 (vgl. Kap. 5.5.2.2).
Die Trennschichtdicke der verwendeten Membran beträgt 43 μm. Diese wurde nach Entnahme der Membran mittels Mikrometerschraube ermittelt und ist Grundlage für die normierte Berechnung der Permabilitäten in barrer. Im Anhang (Kap. 10.6.2) sind die ermittelten Permeationsdaten im einzelnen aufgelistet.
In Tabelle 16 sind die Mittelwerte der Permeationsmessungen (P) und der relative Fehler der Messungen (Standardabweichung /P) für die Membran C3 enthalten.
| Messung Nr. | Gas | P/Nm3·m2·h-1 | Relativer Fehler % | P/Barrer |
| 26(1-3) | CO2 | 2,33E-03 | 9,3 | 209,5 |
| 27(1-3) | CO2 | 1,85E-03 | 3,0 | 166,3 |
| 28(1-3) | H2 | 2,02E-04 | 2,7 | 18,2 |
| 29(1-2) | CH4 | 7,80E-05 | 3,6 | 7,0> |
| 30(1-2) | CO2 | 1,50E-03 | 2,4 | 134,9 |
| 31(1-3) | He | 1,91E-04 | 3,1 | 17,2 |
Wie aus oben stehender Tabelle ersichtlich ist, weist Kohlendioxid von den verwendeten Gasen die höchsten Permeationsraten auf (CO2> H2 ~ He > CH4).
Im Verlauf der 15-tägigen Messung sinkt die mittels Druckanstiegsexperiment gemessene Membranpermeabilität für Kohlendioxid um 35%.
Dieses Verhalten ist vermutlich hauptsächlich auf ein langsames Austrocknen der Membranmatrix zurückzuführen. Wird die Membran angefeuchtet, werden die ursprünglichen CO2-Permeationsraten wieder erreicht (vgl. dazu Experimente im Kap. 7.1.2.2).
Bei Permeationsmessungen mit CO2 sinkt im Messverlauf die Permeabilität kontinuierlich, statt wie bei den anderen verwendeten Gasen stationär zu bleiben (vgl. Abbildung 32), somit liegt für CO2 in der Membran reaktiver Transport vor (vgl. Kap. 7.1.1).
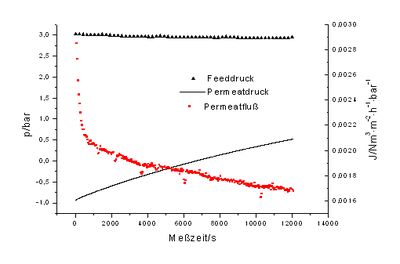
Im Anfangsbereich des Experiments (0-500 s) fällt der Permeatfluß schnell von sehr hohen Werten ab. Dieses Verhalten ist typisch für Membranen, die vorher mit dem Messgas beidseitig bei höheren Drücken in Kontakt waren. Die Membran gibt dann zu Messbeginn in der Membranmatrix gelöste Gase ab. Man hat somit die umgekehrte Situation (Desorption) wie im „time lag“-Experiment (vgl. Abbildung 30). Die Experimente wurden aber diesbezüglich nicht weiter ausgewertet, da die Apparatur für diese Messaufgabe nicht ausgestattet war. Um definierte Startbedingungen zu erhalten und die Desorptions-„time lags“ (vgl. [102]) zu bestimmen, müßte das Evakuieren des Permeatraums durch das öffnen einer Verbindung zu einem definierten evakuierten Volumen (ca. 10 faches Permeatraumvolumen) durchgeführt werden.
Da die CO2-Permeabilität P eine Funktion des Druckverhältnisses Feed/Permeatraum ist, ist die Angabe nur eines Wertes/barrer eine Näherung (vgl. Tabelle 14), die dies nicht berücksichtigt. Um die Größenordnung von Trennfaktoren abschätzen zu können, werden die Permeabilitäten hier näherungsweise als Mittelwert der Permeabilität der ersten 5000 Messsekunden nach dem „time lag“-Bereich berechnet. Für die Ermittlung der Trennfaktoren α wird jeweils die CO2-Permationsrate verwendet, die zeitlich der Messung des zweiten Gases am nächsten lag. Aus Tabelle 14 ergeben sich dann folgende idealen Trennfaktoren α:
| Gase | α | α (max.) | α (min.) |
| CO2/H2 | 9,2 | 11,5 | 7,4 |
| CO2/CH4 | 19,2 | 29,9 | 19,2 |
| CO2/He | 7,8 | 12,2 | 7,8 |
Es sind weiterhin die minimalen bzw. maximalen Trennfaktoren unter Einbeziehung aller Messungen bei gleichen Bedingungen angegeben.
Wie in Kap. 6.3.1 erläutert, sind die Messungen aufgrund von Zellenundichtigkeiten fehlerbehaftet, wenn sehr geringe Permeationsraten bestimmt werden sollen. Dies ist in der vorliegenden Versuchsreihe für die CH4-Permeabilität relevant. Kalkuliert man die gemessenen Werte für die Undichtigkeit mit ein, sind ideale Trennfaktoren CO2/CH4 > 40 realistisch.
Die Bestimmung der Diffusionskoeffizienten und der Gaslöslichkeiten erfolgt mit der „time lag“-Methode.
| P (barrer) | P Mittelwert aus Messung Nr. (Vgl. Kap. ) | D·1011/m2·s-1 | S·102/Ncm3·cm-3 (Polymer)·cmHg-1 | |
| CO2 | 161 | 26.1-3,27.1-3,30.1-2 | 0,99 | 17,8 |
| H2 | 20 | 28.1-4 | > 15 | < 0,13 |
Bei der verwendeten Membrandicke ist die „time lag“-Zeit für Wasserstoff so kurz (< 2 s), dass sie mit der vorhandenen Apparatur nicht Messbar ist. Von daher kann in diesem Falle nur ein Bereich für D angegeben werden.
Die Messungen zeigen, dass die bevorzugte Permeation von CO2 durch die um etwa 2 Größenordnungen bessere Löslichkeit gegenüber H2 bedingt ist und die Diffusion von H2 im Vergleich zu CO2 in der Polymermatrix nur etwa eine Größenordnung schneller ist. Zusammenfassend läßt sich feststellen, dass mit der untersuchten Membran unter identischen Bedingungen höhere Trennfaktoren α (CO2/H2) als mit Nafion-EDAH+ erreichbar sind, jedoch geringere Permeabilitäten. Bei der relativ geringen IEC der Membran ist dies jedoch nur teilweise dem reaktiven Transport zuzuschreiben. Entscheidend sind hier die Eigenschaften des Grundpolymers, dessen gummiartige Struktur hohe CO2-Löslichkeiten ermöglicht und zusätzlich durch seine Ethylenoxidstruktur eine starke Affinität zu CO2 besitzt (vgl. Kap. 3.4).
Auch für die CO2/CH4-Trennung ist das Polymer interessant, seine Transporteigenschaften liegen an der sogenannten „upperbound“ literaturbekannter Verhältnisse von Selektivität zu Permeabilität, wobei bisher nur glasartige und keine gummiartigen Polymere wie das hier untersuchte System mit dieser Eigenschaft bekannt sind (vgl. [109], S. 14).
Membranen der beschriebenen Zusammensetzung besitzen vorteilhafterweise auch gleichzeitig eine gute mechanische (gummiartig, reißfest), filmbildende, thermische (vgl. TGA) und chemische Stabilität (Cl-Gehalt).
7.1.2.2 Membran Typ C1
Bei der Trennschicht der verwendeten Membran handelt es sich um ein Umsetzungsprodukt von Polyepichlorhydrincöthylenoxid mit Polyethylenimin. Dabei beträgt das molare Cl-N Verhältnis 16,5:1 und die IEC 0,43 meq·g-1 (vgl. Kap. 5.5.2.2). Die Trennschichtdicke der Membran C1 beträgt 55 μm.
Im Anhang (Kap. 10.6.3) sind die ermittelten Permeationsdaten im einzelnen aufgelistet.
In Tabelle 17 sind die Mittelwerte der Permeationsmessungen für die Membran C1 enthalten. Aus Spalte 1 ist die Zahl der Messungen (Zahlen in Klammer) unter gleichen Bedingungen ersichtlich.
| Nr. | Gas | Feeddruck/bar | P/Nm3·m2·h-1 | Relativer Fehler/ % | P/Barrer |
| 32(1-3) | CO2 | 3 | 6,46E-03 | 2,0 | 743 |
| 33(1-4) | CO2 | 3 | 6,19E-03 | 1,2 | 712 |
| 34(1-2) | H2 | 3 | 1,34E-03 | 0,0 | 154 |
| 35(1-4) | CH4 | 3 | 4,43E-04 | 0,9 | 51 |
| 36(1-5) | N2 | 3 | 1,10E-04 | 5,4 | 13 |
| 37(1-3) | He | 3 | 4,30E-04 | 1,8 | 49 |
| 39(2-4) | O2 | 3 | 2,19E-04 | 8,1 | 25 |
| 40(1) | N2 | 3 | 9,60E-05 | – | 11 |
| 40(2-3) | H2 | 3 | 4,23E-04 | 0,5 | 49 |
| 41(1) | CO2 | 3 | 1,98E-03 | – | 228 |
| 41(2-3) | CO2 | 3 | 2,14E-03 | 0,0 | 246 |
| 42(1) | CO2 | 3 | 8,31E-03 | 0,0 | 956 |
| 42(2-3) | CO2 | 1 | 8,15E-03 | 1,0 | 937 |
| 43(1) | CO2 | 1 | 8,12E-03 | – | 934 |
| 43(2-3) | H2 | 1 | 3,26E-04 | 3,0 | 37 |
| 44(1) | CO2 | 1 | 7,72E-03 | – | 888 |
| 44(2) | CO2 | 3 | 7,98E-03 | – | 918 |
| 44(3) | CO2 | 10 | 7,94E-03 | – | 913 |
| 44(4) | CO2 | 10 | 8,52E-03 | – | 980 |
| 45(1) | H2 | 1 | 1,59E-03 | – | 183 |
| 45(2) | H2 | 3 | 1,54E-03 | – | 177 |
| 45(3) | H2 | 10 | 1,50E-03 | – | 173 |
| 46(3) | H2 | 1 | 1,58E-03 | – | 182 |
Tabelle 17 enthält die Messungen in chronologischer Reihenfolge. Vor der Messung wurde die Membran in destilliertem Wasser gequollen. Zu Messbeginn ist die Trennschicht der Membran deshalb mit einem dünnen Wasserfilm überzogen. Messung 32-33 zeigt, dass die neü Membran über 2 Messtage relativ konstant hohe Permeationsraten für CO2 aufweist.
Vor der Messung mit Wasserstoff (Nr. 34.1-2) wurde die Membran über Nacht mit trockenem Stickstoff gespült. Die Wasserstoffpermeabilität der so getrockneten Membranmatrix liegt etwa 3-4mal über der der feuchten Membranmatrix (Messung 40-43). Experiment Nr. 35-40.1 mit verschiedenen feuchtegesättigten Gasen zeigt, dass diese alle niedrigere Permeabilitäten als CO2 aufweisen.
Zu Beginn von Experiment 41 war die Membran 19 Tage bei 3 bar Feeddruck und ca. 4 bar Druckdifferenz über die Membran in Betrieb. Die Permeationsrate für Kohlendioxid liegt dabei nur noch bei 30% der ursprünglichen Permeabilität. Als Ursache für diesen Effekt wird die Austrocknung der Membranmatrix vermutet.
Zur Bestätigung dieser Annahme wurden die im folgenden beschriebenen Experimente durchgeführt. Um eine Sättigung des Feedstroms mit Wasserdampf zu gewährleisten wird eine Gasmenge von ca. 750 ml unter Messdruck im Sättiger vorgelegt und vor Messbeginn ca. 1 h unter Rühren temperiert. Bei der Messung wird in der Größenordnung von 10 Nml/min Gas aus diesem Vorrat entnommen, der Druck durch Zuführung trockenen Gases in den Sättiger konstant gehalten. Das Messgas durchströmt vor dem Eintritt in die Messzelle eine Wärmetauscherspirale von 2 m Länge, die sich im gleichen Temperierbad wie die Messzelle befindet. Beim Experiment Nr. 41 wird die Temperatur des Sättigers zum Zeitpunkt 6328 s bei Nr. 41.1 von 30 °C auf 50 °C erhöht, die Temperatur der Messzelle verbleibt bei 30 °C (Nr. 41.2-3.).
In Abbildung 33 sind die so ermittelten Permeabilitäten über die Membran gegen die Messzeit aufgetragen. Wie daraus ersichtlich ist, steigt nach Erhöhung der Sättigertemperatur die Flußrate reproduzierbar an. Dies zeigt, dass die Wasserkonzentration im Feedstrom limitierend für die CO2-Permeabilität ist. Es ist mit diesem Experiment jedoch nicht unterscheidbar, ob es sich um einen gekoppelten Transport von Wasser und CO2 handelt, bei dem die Wasserkonzentration direkt in die Kinetik eingeht, oder um ein Quellungsphänomen, bei dem die Wasserkonzentration im Polymer für den Grad der Quellung verantwortlich ist oder Wasser als Weichmacher wirkt. Aus der Abbildung ist weiterhin ersichtlich, dass der Permeatfluß während des Experimentes jeweils leicht sinkt (reaktiver Transport).
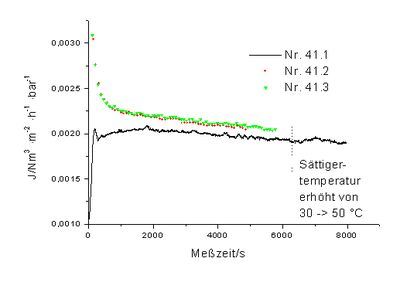
Um festzustellen, ob die anfänglichen Membranpermeabilitäten für CO2 mit dem gleichen Membranmuster nach Befeuchtung wieder erreichbar sind, wurde die Membran C1 in feuchtegesättigtem CO2 bei 1,5 bar Feeddruck und einer Druckdifferenz zum Permeatraum von anfangs 1 bar bei 20 °C 11 Tage stehen gelassen.
Bei der anschließend durchgeführten Messung 42.1 weist die Membran eine Kohlendioxidpermeabilität etwa 28% über dem Startwert (Experiment 32) auf, d.h. die Austrocknung der Membranmatrix ist reversibel. Die im Vergleich zum Startwert gestiegene Permeabilität kann durch Quellung der Membranmatrix in CO2 und das Fehlen des Wasserfilms auf bzw. unter der Trennschicht bedingt sein.
Die folgenden Experimente 42.1-44.1 werden bei einem Feeddruck von 1 bar durchgeführt, dabei werden hohe Trennfaktoren α (CO2/H2) gemessen.
Die Messserien 44-45 dienen der Untersuchung der Druckabhängigkeit der Permeabilität und dabei auftretender Phänomene. Abbildung 34 zeigt den Druckverlauf des Permeationsexperimentes mit CO2.

Die Messdauer bei höheren Feeddrücken ist dadurch limitiert, dass der Permeatdruckaufnehmer einen Messbereich von -1 bis 3 bar besitzt. Zu Beginn einer Messung wird jeweils der Permeatraum evakuiert. In Abbildung 35 sind die aus dem Druckanstieg resultierenden Permeatflüsse normiert auf eine Druckdifferenz von 1 bar aufgetragen. Aus Gründen der übersichtlichkeit sind nur 5% der Messpunkte aufgetragen.

Der Permeatfluß geht bei einem Feeddruck von 1 bar nach etwa 4000 s in den stationären Zustand. Nach etwa 10000 s kommt es aufgrund von Sättigungsphänomenen (reaktiver Transport) zu einem Absinken der Permeationsraten. Mit steigendem Feeddruck steigt auch die Permeabilität für CO2, was auf eine Quellung des Membranmaterials mit CO2 schließen läßt.
Bei 10 bar Feeddruck steigt die Permeationsrate im Messverlauf erst stark an, sinkt dann aber wieder relativ schnell. Da hier aufgrund der noch hohen Druckdifferenz über die Membran das Verhältnis von Feed zu Permeatdruck immer noch sehr hoch ist, kann dieser Effekt nicht allein von der Abhängigkeit des reaktiven Transports vom Druckverhältnis verursacht sein. Dieses Verhalten beruht vermutlich auf einer Austrocknung der Membran im Verlauf des Experiments. Die folgende Permeationsmessung mit H2 (Nr. 45) bestätigt dies, da hier wieder die Permeationsraten für getrocknetes Membranmaterial (vgl. Nr. 34) gemessen werden. Es handelt sich also nicht nur um eine kurzfristige Deckschichtbildung mit einem Wasserfilm oder um Sättigungsphänomene von Carrierpositionen in der Membran.
Die Experimente zeigen, dass die Membranen bei hohen Druckdifferenzen austrocknen. Es kommt hier der Effekt hinzu, dass der Stoffmengenanteil von Wasser im Feed mit zunehmenden Feeddruck im Bereich von 0-10 bar stark sinkt (vgl. Kap. 8) und somit bei Erhöhung des Druckes die Stoffmenge an CO2, die über die Membran transportiert wird, zwar linear zunimmt, die zugeführte Wassermenge aber nicht. In Abbildung 36 ist der Druckverlauf des Permeationsexperimentes 45 gezeigt:

Aus den Messwerten ergeben sich die in Abbildung 37 gezeigten Permeatflüsse.

Die Permeatflüsse verlaufen im Vergleich zu CO2 wesentlich konstanter, d.h. es treten keine Quellungs- oder gekoppelte Transportphänomene auf.
Die normierte Permeabilität für H2 sinkt mit zunehmenden Druck leicht, was auf eine Kompaktierung des Membranmaterials schließen läßt.
Um auszuschließen, dass die höheren Wasserstoffpermeabilitäten bei Messung 45 auf Defekte in der Membran zurückzuführen sind, wurden die im folgenden beschriebenen Bubble-Point-Messungen und Flußmessungen mit variierter Feedüberströmung durchgeführt.
Bei Messung 45.1 wurde zum Zeitpunkt t = 5059 s die überströmung von 3,3 ml/min auf 0 ml/min reduziert, ohne dass eine signifikante änderung auftrat. Es konnte auch bei keiner der vorherigen Messungen eine Abhängigkeit der Permeationsrate von der überströmung festgestellt werden.
Weiterhin wurden mit der Membran nach der Messreihe 45 Bubble-Point-Messungen durchgeführt. Bei der vorliegenden Membran kann mit 11 bar H2 und 15 bar He kein Bubble-Point gefunden werden, d.h. die Membran ist nicht porös.
Aus Tabelle 18 werden folgende ideale Trennfaktoren α für die untersuchte Membran ermittelt.
| Gase | Feeddruck (Bar) | α min. | Messwerte Nr. |
| CO2/H2 | 3 | 4,7(min.),15(max.) | 32,33,34/40 |
| CO2/H2 | 1 | 25(max.) | 43.1-3 |
| CO2/CH4 | 3 | 14,3 | 32,33,35 |
| CO2/N2 | 3 | 56,0 | 32,33,40 |
| CO2/He | 3 | 14,8 | 32,33,37 |
| CO2/O2 | 3 | 29,1 | 32,33,39 |
Die Membran zeigt relativ hohe ideale Trennfaktoren für CO2/H2 sofern sie feucht ist und bei niedrigen Drücken gearbeitet wird. Dann sind die Trennfaktoren auch höher als bei der in Kap. 7.1.2.1 beschriebenen Membran der gleichen Chemie, was mit der höheren IEC korreliert. Die Membran wird aber durch die Erhöhung der IEC für alle Gase permeabler (vgl. Tabelle 13 und Tabelle 17).
Die wirklichen idealen Trennfaktoren für CO2/N2 liegen bei Berücksichtigung der Leckrate der Messzelle > 80.
Zusammenfassend läßt sich sagen, dass mit der untersuchten Membran die in etwa gleichen CO2-Permeabilitäten wie mit Nafion-EDAH+ erreichbar sind, bei dazu im Vergleich nur halber IEC. Die starke Abhängigkeit der Trennfaktoren vom Druck, die mit dem Wassergehalt der Membran korreliert, läßt jedoch erwarten, dass die Trennfaktoren CO2/H2 bei höheren Feeddrücken gegen einen Grenzwert von max. ca. 5 laufen werden.
7.2 Messungen mit Gasgemischen
7.2.1 Anionenaustauscher Typ H3
Bei der Trennschicht der verwendeten Membran handelt es sich um ein Umsetzungsprodukt von Polyepichlorhydrin mit Polyethylenimin. Dabei beträgt das eingesetzte molare Cl-N Verhältnis 8:1. Die aktive Schicht der Membran ist 20 μm dick.
Die Trennfaktoren der Membran werden bei verschiedenen Feeddrücken für Gasgemische und Einzelgase bestimmt.
Für die Ermittlung der Gemischtselektivitäten (CO2:H2 ~ 1:1 bzgl. Volumen, feuchtegesättigt) wird der Permeatraum evakuiert und nach mehreren Stunden beprobt.
Die Trennfaktoren werden aus den GC-Messwerten von Feed und Permeat mittels Gl. 5 berechnet. Nach Versuchsende (20 Tage) wurde die Membran entnommen und die Permeationsraten für feuchtegesättigte Einzelgase mittels Druckanstiegsmethode vermessen. Die idealen Trennfaktoren ergeben sich aus dem Verhältnis der Reingaspermeabilitäten (vgl. Gleichung 38). Im Anhang (Kap. 10.6.4) sind die ermittelten Permeationsdaten im einzelnen aufgelistet. Es ergab sich die folgende Abhängigkeit der Trennfaktoren vom Feeddruck.

Wie oben stehende Abbildung zeigt, sinken die Trennfaktoren bei Erhöhung des Feeddrucks bzw. dem hier experimentell direkt korrelierenden Differenzdrucks über die Membran schnell, um dann in etwa konstant zu bleiben (vgl. dazu auch der Kurvenverlauf Abbildung 46). Der Kurvenverlauf, der sich aus dem Experiment ergibt, stimmt mit dem, nach dem makroskopischen Modell für den Transport in Carrier-Membranen (vgl. Abbildung 12) zu erwartenden, druckabhängigen Verlauf der Permeabilität für die mit dem Carrier reagierende Komponente bzw. dem Trennfaktor überein. Mit zunehmenden Druck verliert der Anteil des Carrier-Transports schnell an Bedeutung.
Die mit Einzelgasen bestimmten Permeationsraten stimmen gut mit denen aus Mischgasmessungen überein, wie dies bei niedrigen Drücken zu erwarten ist.
Wie aus der Messreihe (vgl. Anhang (Kap. 10.6.4), Tabelle 30) ersichtlich ist, braucht die Membran nach der Verwendung bei höheren Drücken einige Zeit, bis bei niedrigen Betriebsdrücken wieder konstante Permeationsraten erreicht werden.
7.2.2 Anionenaustauscher Typ C4
Bei der Trennschicht der Membran handelt es sich um ein Umsetzungsprodukt von Polyepichlorhydrincöthylenoxid mit Polyethylenimin. Dabei beträgt das molare Cl-N Verhältnis 11,9:1, die IEC 0,60 meq·g-1 (vgl. Kap. 5.5.2.2). Die aktive Schicht der Membran ist 60 μm dick.
Mit der Membran werden in einem dreimonatigen Versuchsprogramm Einzelgaspermeabilitäten und Mischgaspermeabilitäten als Funktion von Druck, überströmungsraten und Temperatur ermittelt. Beispielhaft sind Auszüge aus den Ergebnissen im Anhang (Kap. 10.6.5) aufgeführt.
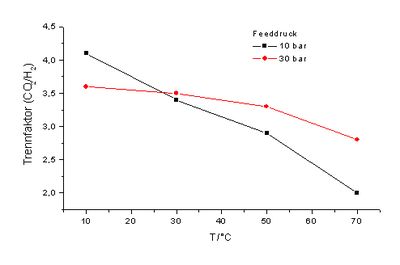
Die untenstehende Abbildung 39 zeigt die Druck- und Temperaturabhängigkeit der Permeationsraten.
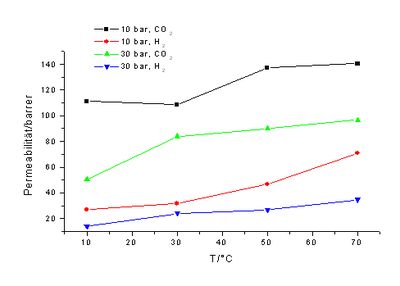
Mit zunehmendem Feeddruck sinken die normierten Permeabilitäten sowohl für CO2 als auch für H2. Die Permeationsraten steigen mit der Temperatur an. Wie aus Abbildung 40 ersichtlich, ist der Anstieg für H2 aber im Verhältnis größer, was zu mit der Temperatur sinkenden Trennfaktoren führt, dieser Effekt wird aber bei zunehmenden Drücken geringer.
7.2.2.1 Bestimmung von Aktivierungsenergien
Aufgrund der Größenordnung von Aktivierungsenergien lassen sich bei Transportprozessen Rückschlüsse auf den Transportmechanismus bzw. den für den Transport geschwindigkeitsbestimmenden Schritt machen. Aus den temperaturabhängigen Permeationsdaten der Membran C4 werden die Aktivierungsenergien mittels eines Arrheniusansatzes [110] bestimmt.
Die scheinbaren Aktivierungsenergien ergeben sich aus der durch lineare Regression ermittelten Steigung b (Ea = – b·R, R = universelle Gaskonstante) aus der Auftragung von ln P gegen T-1 (vgl. Abbildung 12). Der präexponentielle Faktor k0 ergibt sich aus dem Achsenabschnitt a (log k0 = log ea).
Die Permeation von Argon erfolgt in Richtung niedrigeren Partialdrucks entgegen dem Transport von CO2 und H2 aus dem Permeatraum in den Feedraum. Die Permeationsraten sind aus dem Ar-Gehalt des Retentats berechenbar (vgl. Kap. 6.1.3).
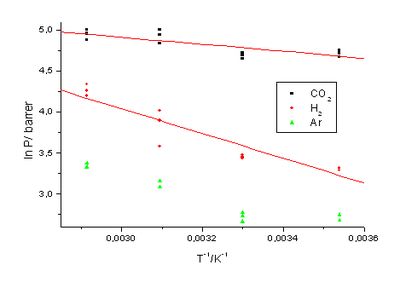
Um zu überprüfen, ob das lineare Modell die experimentellen Daten zufriedenstellend beschreibt, wird ein F-Test durchgeführt, bei dem die Varianz der Messwerte der Regressionsgeraden ins Verhältnis zur Varianz der Messwerte selbst gesetzt wird (vgl. [111], S. 52 und darin zitierte Literatur 41, 42). Ist das Verhältnis der Varianzen sr2/se2 kleiner als der F-Wert, gehorchen die Daten dem Modell der linearen Regression. Die ermittelten Werte für die Aktivierungsenergien und präexponentiellen Faktoren sowie die Vertraünsbereiche sind in Tabelle 19 angegeben.
| Gas | Ea / kJ·mol-1 | log k0 /barrer -1 | sr2/se2 | |
| CO2 | 3,55 ± 0,18 | 2,69 ± 0,03 | 6,10 | 8,02 |
| H2 | 12,54 ± 0,61 | 3,71 ± 0,06 | 4,53 | 8,02 |
| Ar | 8,76 ± 3,10 | 2,76 ± 0,13 | 307,29 | 8,02 |
Die Werte für Argon sind zum Vergleich trotz nicht erfülltem F-Testkriterium angegeben. Analog werden die Versuchsdaten bei 30 bar ausgewertet (vgl. Abbildung 42, Tabelle 20).
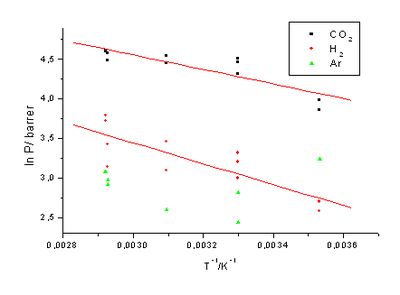
Man erhält die in Tabelle 20 angegebenen Werte für die Aktivierungsenergien.
| Gas | Ea / kJ mol-1 | log k0 / barrer -1 | sr2/se2 | |
| CO2 | 7,62 ± 0,65 | 3,17 ± 0,06 | 6,75 | 9,78 |
| H2 | 10,94 ± 1,81 | 3,21 ± 0,09 | 3,32 | 9,78 |
Die Aktivierungsenergien für die Permeation von CO2 steigen mit Druckerhöhung von 10 auf 30 bar stark an, während die für Wasserstoff nahezu konstant bleiben. Dies läßt auf eine änderung der Polymerstruktur (Verkleinerung der Transportkanäle in der Polymermatrix) schließen, die sich bei größeren Molekülen stärker bemerkbar macht. Eine Erklärungsmöglichkeit für dieses Phänomen ist auch der geringere zu erwartende Wassergehalt bei höheren Drücken im Polymer (vgl. Kap. 8), der zu einer geringeren Quellung und somit zu verkleinerten Transportkanälen führt.
Der Transport von Ar in Gegenrichtung zum CO2– und H2-Transport läßt sich nicht mit einem einfachen Arrhenius-Ansatz beschreiben. Vermutlich liegt hier ein anderer Mechanismus vor.
Literaturbekannte Aktivierungsenergien für die Reaktion von Aminen mit CO2 in wäßrigen Lösungen liegen im Bereich zwischen 38-71 kJ·mol-1[112, 113, 114]. In Tabelle 21 sind Aktivierungsenergien für die Permeation von Gasen durch Polymerfilme angegeben. Für wassergequollene Polymere, die aminfunktionalisiert sind, werden bei niedrigen CO2-Partialdrücken Aktivierungsenergien für die Permeation gemessen, die etwa halb so hoch sind wie die Aktivierungsenergien für die Reaktion von CO2 mit Amin in freier Lösung. Die Aktivierungsenergien für nicht mit der Membranmatrix reagierende Gase liegen aber in der gleichen Größenordnung.
| Polymer/Lösung | Bedingungen | Ea/ kJ·mol-1 |
| Poly(2-(N,N-dimethyl) aminöthyl methacrylate, [43], S. 261 | p(C02): 0,035 bar Feed: Umgebungsdruck 15-45 °C | CO2: 15,7, CH4: 23,8 |
| PVBTAF, [33], S. 55 | p(CO2): 1,25 bar, Feed: 2,75 bar, 23-40 °C | CO2:21,35, H2: 23,78 |
| PDMS, [115], S. 20 | – | CO2:-0,88, N2: 10,76 |
Bei PDMS nehmen die CO2-Permeationsraten mit steigender Temperatur ab, was zu einem negativen Wert für die Aktivierungsenergie führt (siehe auch Kap. 7.2.3)..
Vergleicht man diese Werte mit den Messergebnissen für die untersuchte Membran, gleicht diese von der Charakteristik eher dem gummiartigen PDMS als den aminfunktionalisierten Membranen. Der Transport in diesem Membrantyp bei den untersuchten CO2-Partialdrücken wird also nur unwesentlich durch die Reaktionsgeschwindigkeit Amin-CO2 bestimmt. Die kleinen Aktivierungsenergien deuten eher darauf hin, dass der Transport durch Lösungsvorgänge dominiert wird. Für das leicht kondensierbare Gas CO2 erreicht die Lösungswärme hohe negative Werte, was zu niedrigen Aktivierungsenergien der Permeation führt.
Die zunehmenden Diffusions- und Reaktionsgeschwindigkeiten bei Temperaturerhöhung werden durch die abnehmende Löslichkeit nahezu kompensiert.
7.2.3 Laminate aus PDMS und Anionenaustauschern
Die Trennschicht der untersuchten Membran besteht aus einem Film aus anionenaustauschendem Material und einer darauf laminierten 450 μm dicken PDMS-Schicht (Wacker Elastosil RT601A, additionsvernetzend). Beim Membrantyp H2 wird ein Umsetzungsprodukt von Polyepichlorhydrin mit Polyethylenimin mit einem molaren Cl-N Verhältnis von 4,3:1 und einer von IEC 2,26 meq·g-1 verwendet (vgl. Kap. 5.5.2.2). Die ionenaustauschende Schicht ist 70 μm dick. Zum Vergleich wird die PDMS-Schicht allein vermessen. Die Ergebnisse der Permeationsmessungen sind in Kap. 10.6.6 aufgelistet.
Die Messungen ergeben für äquimolare CO2/H2-Mischungen die in Abbildung 14 gezeigten Permeationsraten. Gemessen wurden die Permeationsraten für PDMS und das Laminat, die Permeationsraten für die ionenaustauschende Schicht (H2) sind nach (Gl. 64) berechnet [14].
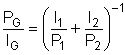
Index: G = Gesamt, 1,2 Teilschichten des Laminats.
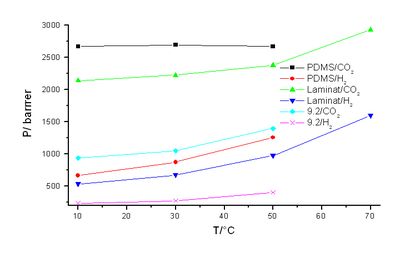
Wie die oben stehende Grafik zeigt, ist die normierte Permeabilität von CO2 durch PDMS am höchsten und bleibt im untersuchten Temperaturbereich nahezu konstant.
Die Permeabilität von PDMS für Wasserstoff nimmt aber mit steigender Temperatur stark zu. Beim Laminat und in der Teilschicht H2 nehmen die Permeabilitäten aller Gase mit der Temperatur zu.
In Abbildung 44 sind die sich aus der Temperaturabhängigkeit der Permeabilitäten ergebenden Trennfaktoren gezeigt.
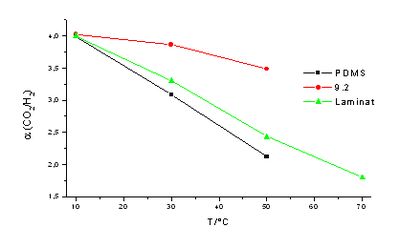
Der Selektivitätsverlust bei Temperaturerhöhung der ionenaustauschenden Schicht fällt wesentlich geringer aus als der von PDMS. Die ermittelten Werte für die Aktivierungsenergien und präexponentiellen Faktoren sind in Tabelle 22 angegeben.
| Membran | Gas | Ea / kJ·mol-1 | Log k0 / barrer -1 |
| PDMS | CO2 | 0,03 | 3,43 |
| PDMS | H2 | 11,94 | 5,02 |
| Laminat | CO2 | 3,99 | 4,05 |
| Laminat | H2 | 14,58 | 5,38 |
| H2 | CO2 | 7,45 | 4,33 |
| H2 | H2 | 10,21 | 4,23 |
Die für PDMS/CO2 ermittelten Werte decken sich im Rahmen der Messgenauigkeit mit Literaturwerten (vgl. Tabelle 23).
Die für H2 ermittelte Aktivierungsenergie für die Schicht H2 liegt im Bereich der in Kap. 7.2.2.1 mit Membranen ähnlicher Chemie ermittelten Werte. Der Wert für CO2 liegt vergleichsweise höher. Als Ursache dafür liegt nahe, dass durch die höhere IEC und den höheren Wassergehalt der Membranschicht H2 der reaktive Transport einen größeren Anteil am Gesamttransport durch die Membran hat, wodurch die Aktivierungsenergie höher wird. Auch die höheren Permeationsraten als bei niedrigerer IEC stützen diese Interpretation. Nachteil der höheren IEC ist aber eine stärkere Quellung der Membran. Im durchgeführten Experiment wellte sich die Membran bei 70 °C mit der Zeit so stark, dass sich das Laminat mit PDMS auftrennte und der Zelldurchgang blockiert wurde.
Die Messungen mit PDMS haben des weiteren gezeigt, dass die Permeabilität dieses Materials nahezu nicht von der Wasserkonzentration im Feed beeinflußt wird (Variation der Sättigertemperatur). Bei Druckerhöhung auf 30 bar (80 Vol% CO2 im Feed) sinken die Permeabilitäten für PDMS auf 1370 barrer und einen Trennfaktor α (CO2/H2) von 2,8 (50 °C: 1,9).
7.3 Widerstandsmessungen
Mit den bezüglich Transporteigenschaften für Gase charakterisierten Materialien werden Widerstandsmessungen durchgeführt, um, wie in Kap. 6.4 diskutiert, Aussagen zur Mobilität geladener Teilchen in der Membran machen zu können.
Die Membranteststücke werden über Nacht im angegebenen Elektrolyt equilibriert, 2 h vor der Messung wird der Elektrolyt ausgetauscht und die Teststücke, von überschüssigem Elektrolyt befreit, zwischen zwei Pt-Elektroden (vgl. Abbildung 29) vermessen. Die Messergebnisse sind im Anhang (Kap. 10.6.7) angegeben.
Mit steigender IEC sinkt der spezifische Widerstand der Membranen (vgl. Abbildung 45). Um einen durchgehenden Ladungstransport durch das Polymer zu gewährleisten, ist eine gewisse minimale IEC notwendig. Unterhalb dieser IEC ist auch beim reaktiven Transport von CO2 (Transportform HCO3–) eine Dominanz der Transporteigenschaften des Grundpolymers zu erwarten. Die niedrigsten ohmschen Widerstände weisen die Membranen bei pH 1 auf, da dann auch die schwach basischen Gruppen als Festionen aktiv sind. Der Widerstand der Membranen ist ebenfalls vom ausgetauschten Gegenion abhängig, generell steigt der Widerstand mit zunehmender Größe des Ions, wobei dieser Effekt mit zunehmender IEC abnimmt.
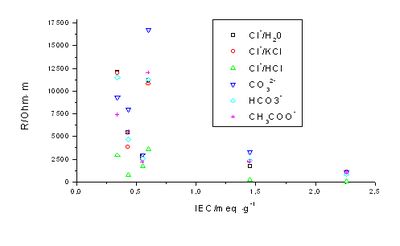
Entscheidend für eine Beurteilung der Membranmatrix bezüglich ihrer Eigenschaften beim reaktiven Transport von CO2 ist deren Widerstand in der HCO3–-Form. Das ausgetauschte Gegenion beeinflußt die Lage der Gleichgewichte bei der Hydrogencarbonatbildung, da diese, wie in Kap. 4.3.3 diskutiert, pH-abhängig sind. Als für den reaktiven Transport günstig hat sich die Verwendung von Anionen, deren konjugierte Säuren einen pKa > 3 aufweisen, herausgestellt [33].
Im Falle der hier vorgestellten Membranen ist es also für den reaktiven CO2-Transport ungünstig, eine Membran in HCl-Form (pH 1) zu verwenden (Gleichgewicht Gl. 24), obwohl diese dann eine höhere verfügbare IEC aufweist.
In Hinsicht auf eine möglichst hohe HCO3–-Mobilität ist also eine hohe stark basische IEC wünschenswert, schwach basische Gruppen stehen nur für den reaktiven Transport über Carbamatbildung zur Verfügung.
Mit Hilfe der Nernst-Einsteinschen-Beziehung lassen sich die in Tabelle 23 angegebenen Diffusionsgeschwindigkeiten der Gegenionen in der Membran aus dem Widerstand bestimmen (vgl. Kap. 6.5). Die Werte zeigen, dass die Mobilität der Hydrogencarbonationen im Vergleich zur Mobilität von CO2 (D aus „time lag“-Messungen, vgl. Kap. 7.1.2.1, Tabelle 16) bei der für die Membranen verwendeten Polymermatrix um 2-5 Größenordnungen kleiner ist. Die Hydrogencarbonatmobilität nimmt mit zunehmender IEC zu, sie korreliert am besten mit der sbIEC.
| Membran | H1 | C1 | H2 | C2 | C3 | C4 |
| IEC/meq·g-1 | 0,55 | 0,43 | 2,26 | 1,45 | 0,34 | 0,6 |
| sbIEC/meq·g-1 | 0,42 | 0,22 | 1,34 | 0,56 | 0,19 | 0,45 |
| wbIEC/meq·g-1 | 0,13 | 0,21 | 0,92 | 0,58 | 0,15 | 0,15 |
| Gegenion | ||||||
| Cl–/H20 dest. | 3,17E-13 | 1,47E-13 | 5,61E-13 | 3,30E-13 | 9,11E-14 | 5,35E-14 |
| Cl–/0,1 m KCl | 3,58E-13 | 2,08E-13 | 4,22E-13 | 2,53E-13 | 9,17E-14 | 5,54E-14 |
| Cl–/0,1 m HCl | 5,20E-13 | 1,12E-12 | 9,24E-12 | 2,79E-12 | 3,78E-13 | 1,66E-13 |
| CO32- | 2,96E-13 | 1,00E-13 | 4,31E-13 | 1,72E-13 | 1,19E-13 | 3,58E-14 |
| HCO3– | 8,61E-15 | 4,38E-15 | 8,04E-14 | 1,44E-14 | 6,72E-16 | 9,83E-16 |
| CH3COO– | 4,03E-13 | 1,44E-13 | 4,56E-13 | 2,54E-13 | 1,49E-13 | 4,97E-14 |
Die vergleichsweise geringe Mobilität von Hydrogencarbonat in der Membranmatrix, die sich aus den Widerstandsmessungen ergibt, ist ein weiterer Beleg für die in Kap. 7.2.2 aufgrund der Aktivierungsenergien getroffenen Aussage, dass beim Transport von CO2 durch die hier vorgestellten Umsetzungsprodukte von Polyepichlorhydrin und Polyethylenimin der reaktive Transport in Form von Hydrogencarbonat nur eine untergeordnete Rolle spielt.
Die Synthese von Membranen hoher Hydrogencarbonatmobilität (geringer ohmscher Widerstand für HCO3–) bei gleichzeitig akzeptablem Quellungsverhalten erfordert die Verwendung kurzkettiger Diamine zusätzlich zum Polyethylenimin. Die dann entstehenden Polymere verlieren aber ihren gummiartigen Charakter und die damit verbundenen Vorteile mit steigender Vernetzung.
Wie aus Abbildung 45 hervorgeht, liegt der Widerstand der Carbonatform einer Membran im allgemeinen über dem der Hydrogencarbonatform. Da aus Carbonat und CO2 Hydrogencarbonat entsteht, müßte sich der Widerstand einer Membran in der Carbonatform, wenn sie einer CO2-Atmosphäre ausgesetzt wird, dem der Hydrogencarbonatform nähern. Durch die Festlegung von Randbedingungen wie Membran- und Elektrodengeometrie, Druck und Temperatur wäre es denkbar, so Aussagen zu Transport- und Reaktionsvorgängen in der Membranmatrix zu erhalten.
Versuche mit der vorhandenen Messzelle mit verschiedenen Anionenaustauschermembranen haben jedoch gezeigt, dass belastbare Ergebnisse mit dieser Methode nur mit höherem experimentellen Aufwand erzielbar sind. Ein Problem dabei ist die Gewährleistung eines konstanten Wassergehaltes in der Membran während des Experimentes, da der Membranwiderstand sehr stark von diesem abhängt.
Weitere Widerstandsmessungen werden mit Kationenaustauschermembranen in der EDAH+-Form durchgeführt.
| Membran | IEC/ meq·g-1 | wc/% | T/°C | R/Ω·m | D/m2·s-1 |
| SPEEK-EDAH+ (Kap. ) | 1,35 | 80 | 22 | 5,30 | 6,62E-11 |
| Nafion-EDAH+ (Kap. ) | 0,9 | 11 | 25 | 5,88 [80] | 5,7E-11[80, S. 4784 ], 5E-11[34, S. 342] |
Mit den Literaturwerten für Nafion-EDAH+ kann die Vergleichbarkeit der Mess- und Auswertemethode bestätigt werden.
Auch bei den kationenaustauschenden Polymeren nimmt der Membranwiderstand mit zunehmender IEC ab (Untersuchungsmaterial: Serien von Polymeren aus SPEEK vgl. Kap. 5.4.2.2). Aus dem Vergleich der Mobilitäten von HCO3– in Anionenaustauschermaterialien und EDAH+-Carriern in Kationenaustauschern ist ersichtlich, warum mit mobilen Carriern im Vergleich zu fixierten Carriern höhere Permeationsraten beim reaktiven Transport möglich sind (vgl. Kap. 3.7).
Die Verwendung von SPEEK hat gegenüber Nafion den Vorteil, dass höhere IEC’s realisierbar sind und damit höhere Permeabilitäten. Des weiteren sind die Materialien vernetzbar und damit die Quellung und die mechanische Stabilität kontrollierbar.
Auf eine ausführliche experimentelle Untersuchung dieser Materialien im Rahmen dieser Arbeit wurde jedoch verzichtet, da durch die Austrocknung bei höheren Drücken auch immer Carrierverluste auftreten. Potentiell sind SPEEK-Polymere für Carrier-Membranen mit Einsatzbereich Drücke < 3 bar aber sehr gut geeignet, da durch die Reaktivität (vgl. Kap. 5.4.2.1) der Polymerkette Substitutionsmuster entstehen, die zu relativ großen Abständen zwischen den einzelnen funktionellen Gruppen führen.
Durch den aromatischen Charakter der Polymerhauptkette weist diese eine hohe Steifigkeit auf, so dass bei Vernetzung über die funktionellen Gruppen relativ große Kanäle auf molekularer Ebene in der Polymermatrix entstehen. Aufgrund dieser Struktur sind dann auch für Carrier mit höheren Molekulargewichten akzeptable Mobilitäten realisierbar. Für CO2-Carrier-Membranen ist somit auch der Einsatz anderer Amine als EDAH+ denkbar (vgl. Kap. 4.3.3). Amine höherer Molmassen haben im allgemeinen höhere Siedepunkte und sind somit als Carrier weniger flüchtig, was zu höheren Membranstandzeiten führt.
